
Содержание
Количество ионов в соединении зависит от структуры соединения и степени окисления элементов в нем. Число окисления элемента - это количество электронов, которое атом имеет или нуждается в нем относительно количества протонов в его ядре. Это определяет ионный заряд атома, что важно для описания ионных соединений, которые он образует с другими атомами
направления
-
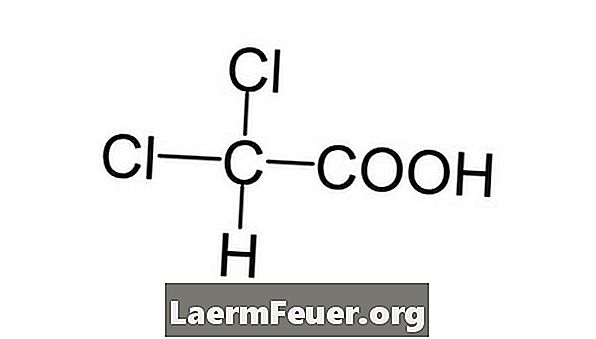
Напишите химическую формулу для рассматриваемого соединения.
-
Определите многоатомные ионы в соединении. Многоатомные ионы - это ионные молекулы, состоящие из более чем одного атома (обычно более одного элемента). См. Ссылки на список общих многоатомных ионов и их зарядов.
-
Разделите катионы и анионы. Катионы - это положительно заряженные ионы, анионы - отрицательно заряженные ионы. Например, FeSO (4) (сульфат железа (II)) содержит катион железа (Fe + 2) и анион сульфат (SO (4) -2). Важно отметить, что сульфат - это многоатомный ион, а не набор из пяти разных ионов. Римская цифра «II» обозначает степень окисления железа +2. Это позволяет ему связываться только с одним сульфатным анионом.
Если химический символ имеет показатель степени, связанный с ним, в соединении есть несколько атомов этого элемента. Если они не являются частью многоатомного иона, каждый атом этого элемента является отдельным ионом. Например, сульфат железа (III) записывается как Fe2 (SO4) 3. Степень окисления +3 для железа требует различного количества сульфатов на ионную связь. В этом случае два иона железа (III) будут связываться с тремя сульфат-ионами.
-
Добавьте общее количество катионов и анионов. Например, сульфат железа (II) имеет два иона: катион железа и сульфат-анион.
чаевые
- Полное понимание показателей окисления поможет вам быстро и уверенно расшифровать ионную природу соединения.
Что вам нужно
- Периодическая таблица