
Содержание
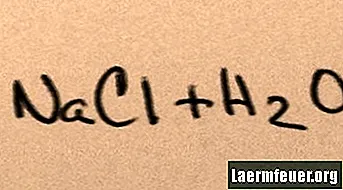
Когда соль добавляется в воду, она растворяется в составляющих ее молекулах до тех пор, пока максимальное количество ионов соли, которые вода может поддерживать, не будет плавать вокруг молекул водорода и кислорода. Когда это происходит, раствор называют «насыщенным». Когда растворяется больше соли, ионы натрия и хлора сталкиваются друг с другом и рекомбинируют в кристаллах соли. Это явление известно как «осадки», потому что образовавшееся твердое вещество падает на дно воды. Соли «гидрофильны», то есть их привлекает вода. Этот аттракцион способствует знакомой форме выпадения осадков: капли дождя образуются вокруг крошечных кристаллов соли в облаках, что придает им слегка соленый вкус.
Основа

Электролиты

Соль не проводит электричество в твердом состоянии, но в жидком (жидком) состоянии она образует раствор, который очень хорошо проводит электричество. Электропроводность зависит от типа используемой соли, но эти жидкости, называемые растворами электролитов, являются отличными переносчиками соединений, необходимых человеческому организму. Электрические импульсы, генерируемые мозгом, производят свободный кислород, который используется кровью. Молекулы соли подразделяются на электролиты (натрий, калий или кальций) и хлориды в растворе: хлорид перекачивается кровью и почками в мочу, а электролиты распределяются по нервно-мышечной системе в процессе, который спортсмены называют регидратация.
Коллигативные свойства

Любой раствор отличается от исходного состава, потому что добавление молекул, даже если они не образуют новых соединений, изменяет молекулярный вес жидкости и влияет на ее свойства. Соленая вода плотнее чистой, а также медленнее замерзает. Однако при замерзании соль перемещается к пределам жидкости, делая ее более тяжелой и насыщенной, а затем понижая ее точку замерзания. На другом конце состояния вещества, чем плотнее соленая вода, тем больше тепла требуется для испарения, пока вода не вытечет, оставив слой соли. Повара ждут, пока вода в кастрюле закипит, чтобы добавить соль, чтобы не задерживать нагрев. Эти качества, известные как «коллигативные свойства», помогают ученым определять молекулярный вес соленой воды. Если можно измерить массу, атмосферное давление и точку кипения жидкости, ученые могут вычесть молекулярную массу воды, чтобы узнать, какие соли присутствуют.